আজকে আমরা জানবো আইসোটোপ কাকে বলে? এই প্রশ্নের উত্তর পেতে আমাদের এই পোস্টটি সম্পূর্ণ পড়ুন। আশা করি আপনারা এই প্রশ্নের উত্তর ভালো ভাবে বুঝতে পারবেন।
আইসোটোপ কাকে বলে? উদাহরণসহ সংজ্ঞা, আইসোটপের ব্যবহার, আইসোবার কাকে বলে?, আইসোটোন কাকে বলে?

আইসোটোপ কাকে বলে?
যেসকল মৌলের বিভিন্ন ধরনের পরমাণু থাকে এবং এদের প্রোটন বা পারমাণবিক সংখ্যা সমান কিন্তু ভর সংখ্যা ভিন্ন হয় তাদেরকে ওই সকল মৌলের আইসোটোপ বলে।
অন্য ভাবে সংজ্ঞা দিলে এভাবে দেওয়া যায়: যে সকল পরমাণুর প্রোটন সংখ্যা সমান কিন্তু বাকি সংখ্যা ভিন্ন ভিন্ন হয় তাদেরকে বলা হয় আইসোটোপ।
মনে রাখার সহজ কৌশল: উপরের যেকোনো একটি সংজ্ঞা ২০ বার পড়ুন। তাহলে দেখবেন এমনিতে মনে থাকছে। ❤️
উদাহরণ: কার্বন এর উদাহরণস্বরূপ, তিনটি প্রধান ইসোটোপ রয়েছে – কার্বন-১২ (প্রোটন ১২, নিউট্রন ০), কার্বন-১৩ (প্রোটন ১৩, নিউট্রন ০) এবং কার্বন-১৪ (প্রোটন ১৪, নিউট্রন ০)।
আইসোটোপ গুণগত বৈশিষ্ট্য পরিবর্তনের ফলে, তাদের ব্যবহার বিভিন্ন ক্ষেত্রে প্রযোজ্য হয়। উদাহরণস্বরূপ, কার্বন-১৪ রেডিওকার্বন ডেটিং (carbon dating) এর জন্য ব্যবহৃত হয়, প্রোটিয়াম-১০১ এ ব্যবহার হয় রাসায়নিক গবেষণা ও ক্যান্সার চিকিৎসায়, ইটয়ের জন্য বিভিন্ন প্রকারের সমষ্টি বা কমিউনিটি তৈরি করার সময় ভিন্ন আইসোটোপ ব্যবহার হয়।
উদাহরণ স্বরূপ- বেশিরভাগ কার্বনের পরমাণু ৬টি প্রোটন এবং ৬টি নিউট্রন থাকে। কিন্তু কার্বনের কিছু পরমাণুতে ৮টি বা ৭টি নিউট্রন থাকে। আর সেজন্য বলা হয় কার্বন এ তিনটি আইসোটোপ থাকে।
আইসোটোপ বলতে কি বোঝায়?
একই মৌলের বিভিন্ন পরমাণুর পরমাণু-ক্রমাঙ্ক একই কিন্তু নিউক্লিয়াসে ভিন্ন সংখ্যক নিউট্রন থাকার জন্য ভরসংখ্যা আলাদা হলে, তাদের পরস্পরকে আইসোটোপ (Isotope) বা সমস্থানিক বলে।
Also Read: ভাষা কাকে বলে?
হাইড্রোজেনের আইসোটোপ কি?
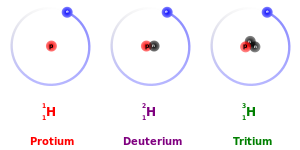
হাইড্রোজেনের তিনটি আইসোটোপ –
- প্রোটিয়াম 1H1
- ডিউটেরিয়াম 1H2
- ট্রিটিয়াম 1H3
আইসোটোপ
আইসোটোপ: কোন মৌলের ভিন্ন ধরনের পরমাণু যাদের পারমাণবিক বা প্রোটন সংখ্যা সমান কিন্তু ভরসংখ্যা ভিন্ন তাদেরকে ঐ মৌলের আইসোটোপ বলে।
একটি মৌলের প্রতিটি পরমাণুতে নির্দিষ্ট সংখ্যক প্রোটন ও ইলেকট্রন থাকে। কিন্তু একটি মৌলের সকল পরমাণুর ভর এক নাও হতে পারে। কারণ মৌলের পরমাণুতে বিভিন্ন সংখ্যায় নিউট্রন থাকতে পারে।
উদাহরণ হিসেবে বলা যায়, হাইড্রোজেনের সকল পরমাণুতে একটি করে প্রোটন ও ইলেকট্রন থাকে। নিচের চিত্র গুলো ভালো করে লক্ষ্য কর-
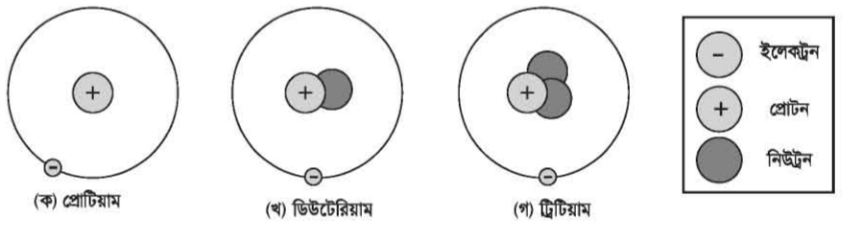
(ক চিত্র) হাইড্রোজেনের বেশিরভাগ পরমাণুতে কোনো নিউট্রন নেই, তাই এদের ভরসংখ্যা ১
কিন্তু (খ) চিত্রের পরমাণুটির মতো হাইড্রোজেনের কিছু পরমাণুতে একটি নিউট্রন থাকে, এদের ভরসংখ্যা ২
(গ) চিত্রের পরমাণুটির মতো হাইড্রোজেনের কিছু পরমাণুতে দুটি নিউট্রন থাকে, এদের ভরসংখ্যা ৩
চিত্রের তিনটি পরমাণু হাইড্রোজেনের তিনটি আইসোটোপ। একইভাবে, কোন মৌলের ভিন্ন ধরনের পরমাণু যাদের পারমাণবিক বা প্রোটন সংখ্যা সমান কিন্তু ভরসংখ্যা ভিন্ন তাদেরকে ঐ মৌলের আইসোটোপ বলে।
Also Read: ব্যবস্থাপনা কাকে বলে?
আইসোটোপ এর ধর্ম কি?
আইসোটোপের ধর্ম নিম্নে দেয়া হল-
- আইসোটোপ স্থায়ী হয়।
- আইসোটোপবিভিন্ন তেজস্ক্রিয় রশ্মি ও কণা বিকিরণ করে থাকে।
Also Read: রাষ্ট্রবিজ্ঞান কাকে বলে?
আইসোটোপ এর বৈশিষ্ট্য কি?
আইসোটোপ এর কিছু বৈশিষ্ট্য রয়েছে। আর এই বৈশিষ্ট্যগুলো কে কেন্দ্র করে আইসোটোপ এর পরিচয় পাওয়া যায়। সুতরাং নিম্নে কিছু বৈশিষ্ট্য উপস্থাপন করা হলো-
- আইসোটোপের পারমাণবিক সংখ্যা সমান কিন্তু ভর সংখ্যা ভিন্ন হয়।
- আইসোটোপ এর ভর,গলনাঙ্ক,ঘনত্ব,স্ফুটনাঙ্ক ইত্যাদি উপাদান গুলির ভৌত ধর্ম সব সময় পৃথক হয়।
- আইসোটোপ এর ক্ষেত্রে একই মৌলের পর্যায় সারণী একই অবস্থানে থাকে।
- আইসোটোপের রাসায়নিক ধর্ম যোজ্যতা ইলেকট্রন সব সময় অভিন্ন থাকে।
আইসোটোপ এর ব্যবহার
নিম্নে আইসোটোপের ব্যবহার দেয়া হলো-
- মাটির মধ্যে থাকা বিভিন্ন ফসলের বয়স নির্ণয় করে থাকে আইসোটোপ।
- আইসোটোপ পতঙ্গ নিয়ন্ত্রণে রাখে।
- আইসোটোপের সাহায্যে তেজস্ক্রিয় কার্বন এর মাধ্যমে পুরাতন শিলা,গাছ এবং পৃথিবীর বয়স নির্ণয় করা যায়।
- কোবাল্টের আইসোটোপ ক্যান্সার কোষ এবং ম্যালিগন্যান্ট টিউমার কোষ ধ্বংস করতে সাহায্য করে।
- ফসলে কোন ধরনের সার কতটুকু পরিমাণে ব্যবহার করতে হবে তা নির্ণয় করতে আইসোটোপ সাহায্য করে।
- ডাক্তারি সকল যন্ত্রপাতি জীবাণুমুক্ত করতে আইসোটোপ ব্যবহার করা হয়।
- মানবদেহে যদি কোন ক্ষুদ্র রক্তনালী ক্ষতিগ্রস্ত হয় তা সনাক্ত করতে আইসোটোপ ব্যবহার করা হয়।
- মানবদেহের বিভিন্ন রোগ নির্ণয় এবং নিরাময় করতে আইসোটোপ ব্যবহার করে থাকে।
- চিকিৎসা ক্ষেত্রে ক্যান্সার এবং টিউমার চিকিৎসাযর জন্য তেজস্ক্রিয় আইসোটোপ (১৩১) ব্যবহার করা হয়।
- কৃষিক্ষেত্রে আইসোটোপ ব্যবহার করে উদ্ভিদের বৃদ্ধি ও রোগ সম্পর্কে বিভিন্ন তথ্য জানা যায়।
- বিভিন্ন ধরনের রাসায়নিক বিক্রিয়ার গতি প্রকৃতি নির্ণয় এর জন্য তেজস্ক্রিয় আইসোটোপ (C13 , N15 , O18 , S35 ইত্যাদি) ব্যবহার করা হয় ।
- খাদ্য ও ফলমূল সংরক্ষণে আইসোটোপ ব্যাকটেরিয়া সহ অনেক ধরনের জীবাণু ধ্বংস করে থাকে।
চিকিৎসা ক্ষেত্রে তেজস্ক্রিয় আইসোটোপের ব্যবহার গুলো লেখ
চিকিৎসা ক্ষেত্রে বিভিন্নভাবে তেজস্ক্রিয় আইসোটোপ ব্যবহার করা হয়ে থাকে। সেগুলো সুন্দর ভাবে পরিবেশন করা হলো:
- কোবাল্টের আইসোটোপ ব্যবহার করে টিউমার নিরাময় করা হয় এছাড়াও টিউমার শনাক্তকারী হয়ে আইসোটোপ ব্যবহার করা হয়ে থাকে।
- ইরিডিয়াম নামক এক ধরনের পরমাণুর আইসোটোপ ব্যবহার করে ক্যান্সার নিরাময় করা হয়ে থাকে এছাড়াও কেমোথেরাপির কাজে ব্যবহার করা হয় ।
- টেকনিশিয়ান 99 নামের এক ধরনের আইসোটোপ হয়েছে যেটি ব্যবহার করে শরীরের ভেতর ছবি তোলা হয়ে থাকে । মূলত শরীরের একটি নির্দিষ্ট অংশের ছবি ধারণ করার জন্য সর্বপ্রথম সেই স্থানে টেকনিসিয়াম 99 আইসোটোপের ইনজেকশন পুশ করা হয়। অতঃপর সেখান থেকে তেজস্ক্রিয় রশ্মি বের হতে থাকে । মূলত সেই সকল তেজস্ক্রিয় রশ্মি শনাক্ত করে নির্দিষ্ট অংশের ভেতর কার ছবি তোলা হয় । সাধারণত টেকনিশিয়ান 99 আইসোটোপের লাইফটাইম হয়ে থাকে 6 ঘন্টা বা তার বেশি ।
- এছাড়াও থাইরয়েড রোগ সনাক্ত এবং থাইরয়েড রোগ নিরাময় করার জন্য আয়োডিনের এক ধরনের আইসোটোপ ব্যবহার করা হয়ে থাকে ।
- অক্সিজেনের আইসোটোপ ব্যবহার করে শ্বাসকষ্ট রোগের আক্রান্ত রোগীদের চিকিৎসা প্রদান করা যেতে পারে । যদিও সেটি অনেক ব্যয়বহুল ।
- মানবদেহের ক্ষতিগ্রস্ত কোষ নিরাময় করার ক্ষেত্রে বিভিন্ন পদার্থের আইসোটোপ ব্যবহার করা হয়ে থাকে । তবে ক্যান্সার জটিলতায় আক্রান্ত কোষগুলো নিরাময়ের ক্ষেত্রে এটি ব্যবহার সবচেয়ে বেশি ।
আইসোটোন কি বা কাকে বলে?
যেসকল পরমাণুর নিউট্রন সংখ্যা সমান কিন্তু প্রোটন সংখ্যা ভিন্ন তাদের আইসোটোন বলে। আইসোটোন ভিন্ন ভিন্ন মৌলের পরমাণুর ক্ষেত্রে হয়ে থাকে। যেমন – 7N15, 6N14
ভর সংখ্যা = প্রোটন সংখ্যা + নিউট্রন সংখ্যা
আইসোবার কী?
যেসকল পরমাণুর ভর সংখ্যা সমান কিন্তু প্রোটন সংখ্যা ভিন্ন, তাদের আইসোবার বলে। আইসোবার ভিন্ন ভিন্ন মৌলের পরমাণুর ক্ষেত্রে হয়ে থাকে। যেমন – 26Fe58 ও 27N58.
রেডিও আইসোটোপ কি?
যেসকল আইসোটোপ সামান্য সময়ের জন্য কৃত্রিম তেজস্ক্রিয়তা প্রদর্শন করে তাদের রেডিও আইসোটোপ বলা হয়। যেমন – ইউরেনিয়াম,প্লুটোনিয়াম, রেডিয়াম, ইত্যাদি।
রেডিও আইসোটোপের ব্যবহার –
- কৃষিক্ষেত্রে কীটপতঙ্গ ধ্বংস করা
- ক্যান্সার নিয়াময়ের জন্য
- টিউমারের জন্য ইত্যাদি ক্ষেত্রে রেডিও আইসোটোপ ব্যবহার করা হয়।
- এগুলো ছাড়াও গবেষণাকার্যে ও শিল্পবিজ্ঞানে রেডিও আইসোটোপের ব্যবহার রয়েছে
- অধিক ফসল উৎপাদন
- বীজ সংরক্ষণ ইত্যাদি।
আইসোমার কি? উদাহরণ দাও
যেসকল পরমাণুর পারমাণবিক সংখ্যা এবং ভর সংখ্যা একই কিন্তু তাদের অভ্যন্তরীণ গঠন ভিন্ন, তাদেরকে পরস্পরের আইসোমার বলে। যেমন – ইথানল, ডাই মিথাইল ইথাইল ইত্যাদি।
আইসোটোপ ও আইসোবারের মধ্যকার পার্থক্য কী ?
আইসোবার একটি আবহাওয়া মানচিত্রে আঁকা সমান বায়ুমণ্ডলীয় চাপের কাল্পনিক রেখা। প্রতিটি লাইন একটি নির্দিষ্ট মানের চাপ দিয়ে যায়, নির্দিষ্ট নিয়মগুলি অনুসরণ করা হয়। আইসোবার লাইনগুলি কখনই একে অপরকে অতিক্রম বা স্পর্শ করতে পারে না।
আইসোবার রেখা গুলো যেমন ৯৯২, ৯৯৬, ১০০০ মিলিবার এর চাপ দিয়ে যেতে পারে (প্রতি ৪ মিলিবার অন্তর) । এটি আবহাওয়াবিদদের পাশাপাশি স্থানীয় বায়ু নিদর্শনগুলির পূর্বাভাস দেওয়ার সুযোগ দেয়।
এটা রসায়ন এবং পদার্থ বিজ্ঞানের বিষয়। সাধারনতঃ একটি পরমানুর নিউক্লিয়াসে নির্দিষ্ট সংখ্যক প্রোটন এবং সমপরিমান নিউট্রন থাকে। এর পারমাণবিক সংখ্যা একটাই। তবে কোন কোন মৌল পদার্থের নিউক্লিয়াসে অধিক সংখ্যক নিউট্রন থাকলে তার পারমানবিক সংখ্যা এক হলেও পারমাণবিক ওজন ভিন্ন হয়। এমন সব রাসায়নিক উপাদানগুলির দুটি বা ততোধিক কোন রূপ রয়েছে। এগুলোকে ঐ মৌলের আইসোটোপ বলে।
হাইড্রোজেনের কোন আইসোটোপ তেজস্ক্রিয়তার মাধ্যমে তৈরি হয়?
হাইড্রোজেন এর তেজস্ক্রিয় আইসোটোপ টি হলো ট্রিটিয়াম(H3)। যার নিউক্লিয়াস এ একটি প্রোটন ও দুটি নিউট্রন থাকে। অন্য দিকে হাইড্রোজেন H1 আইসোটোপ এ একটি প্রোটন এবং H2 আইসোটোপ এ একটি প্রোটন ও একটি নিউট্রন থাকে। প্রকৃতি তে H3 বিরল অবস্থায় পাওয়া যায়। চিকিৎসা শাস্ত্রে ট্রিটিয়াম রেডিও এক্টিভ ট্রেসার হিসেবে ব্যবহার করা হয়। এছাড়াও এটি নিউক্লিয়ার ফিউশন এ ব্যবহার করা হয়। নিউক্লিয় বিভাজনের মাধ্যমে ট্রিটিয়াম ভেঙে হিলিয়াম এ পরিনত হয়।
নিউক্লিয় সংযোজন বিক্রিয়ায় ট্রিটিয়াম ও ডয়টরিয়াম এর সংযোজন এর ফলে হিলিয়াম, নিউট্রন ও প্রচুর শক্তি নির্গত হয় যার মান ১৭.৬ মেগা ভোল্ট।